热力学第一定律是能量守恒原理的一种表达方式。此定律曰:在一个热力学系统内,能量可转换,即可从一种形式转变成另一种形式,但不能自行产生,也不能毁灭。一般公式化为:一个系统内能的改变等于供给系统的热量减去系统对外环境所作的功。 热力学第一定律是生物,物理化学等学科的重要定律。
中文名称:热力学第一定律
外文名称:the first law of thermodynamics
应用学科:物理
提出时间:19世纪50年代
提出者:迈耳 J.R.Mayer、焦耳 T.P.Joule
表达式:△U=Q+W
基本介绍
热力学第一定律:△U=Q+W。系统在过程中能量的变化关系
英文翻译:the first law of thermodynamics
定律简单解释
在热力学中,系统发生变化时,设与环境之间交换的热为Q,与环境交换的功为W,可得热力学能(亦称内能)的变化为
ΔU = Q+ W
或Q=ΔU-W(目前通用这两种说法,以前一种用的多),为了避免混淆,物理中普遍使用第一种,而化学中通常是说系统对外做功,故会用后一种。
自然界一切物体都具有能量,能量有各种不同形式,它能从一种形式转化为另一种形式,从一个物体传递给另一个物体,在转化和传递过程中能量的总和不变。
英文翻译:The first explicit statement of the first law of thermodynamics, by Rudolf Clausius in 1850, referred to cyclic thermodynamic processes
"In all cases in which work is produced by the agency of heat, a quantity of heat is consumed which is proportional to the work done; and conversely, by the expenditure of an equal quantity of work an equal quantity of heat is produced."
基本内容
热可以转变为功,功也可以转变为热;消耗一定的功必产生一定的热,一定的热消失时,也必产生一定的功。
普遍的能量转化和守恒定律是一切涉及热现象的宏观过程中的具体表现。热力学的基本定律之一。
热力学第一定律是对能量守恒和转换定律的一种表述方式。
表征热力学系统能量的是内能。通过作功和传热,系统与外界交换能量,使内能有所变化。根据普遍的能量守恒定律,系统由初态Ⅰ经过任意过程到达终态Ⅱ后,内能的增量ΔU应等于在此过程中外界对系统传递的热量Q 和系统对外界作功A之差,即UⅡ-UⅠ=ΔU=Q+W或Q=ΔU-W这就是热力学第一定律的表达式。如果除作功、传热外,还有因物质从外界进入系统而带入的能量Z,则应为ΔU=Q+W+Z。当然,上述ΔU、W、Q、Z均可正可负(使系统能量增加为正、减少为负)。对于无限小过程,热力学第一定律的微分表达式为
dU=δQ+δW因U是状态函数,dU是全微分;Q、W是过程量,δQ和δW只表示微小量并非全微分,用符号δ以示区别。又因ΔU或dU只涉及初、终态,只要求系统初、终态是平衡态,与中间状态是否平衡态无关。 对于准静态过程,有δQ=dU+pdV
表述
热力学的基本定律之一,是能量守恒和转换定律的一种表述方式。热力学第一定律指出,热能可以从一个物体传递给另一个物体,也可以与机械能或其他能量相互转换,在传递和转换过程中,能量的总值不变。它的另一种表述方式为:不消耗能量就可以作功的"第一类永动机"是不可能实现的。
18世纪以来,流行一时的"热质说"相继为 Count von朗福德、J.R.von迈尔、J.P.焦耳等人所推翻。他们证明热是物质运动的一种表现,并逐步归纳成第一定律的表述方式。其中焦耳于1840~1850年进行的热功当量实验为这一定律的科学表述奠定了基础。焦耳的实验表明,机械能所作的功W与其转换得到的热量Q之间存在着严格的数量关系,不管转换的过程如何,一个单位的热量永远相当于E个单位的功,即W=EQ,式中E称为热功当量。在国际单位制(SI)中热量和功的单位都是焦耳(J),所以E=1。
对于封闭系统(见热力系统),热力学第一定律可表达为
Q=ΔU +W
或 δQ=dU +δW
它表明向系统输入的热量Q,等于系统内能的增量ΔU 和系统对外界作功W之和。
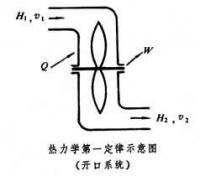
在热工设备中经常遇到工质稳定地流入和流出设备的开口系统(见图)的情形。这时,热力学第一定律可表达为
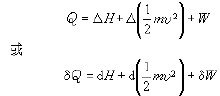
它表明向系统输入的热量Q,等于质量为 m的流体流经系统前后焓H 的增量、动能
的增量以及系统向外界输出的机械功W之和。

 更多
更多
 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底