第一电离能是基态的气态原子失去最外层的一个电子所需能量。第一电离能数值越小,原子越容易失去一个电子;第一电离能数值越大,原子越难失去一个电子。
中文名:第一电离能
外文名:The first ionization energy
定 义:原子失去最外层一个电子所需能量
应用学科:化学 物理
单 位:kJ/mol
名词解释
电离能意义
电离能可以衡量元素的原子失去一个电子的难易程度(可近似理解为金属性)。
表达式
第一电离能的符号为I1,单位是kJ/mol。气态原子形成+1价气态阳离子的过程可表示为:
M(g) ― e- → M+ (g)(任何形态都一样)
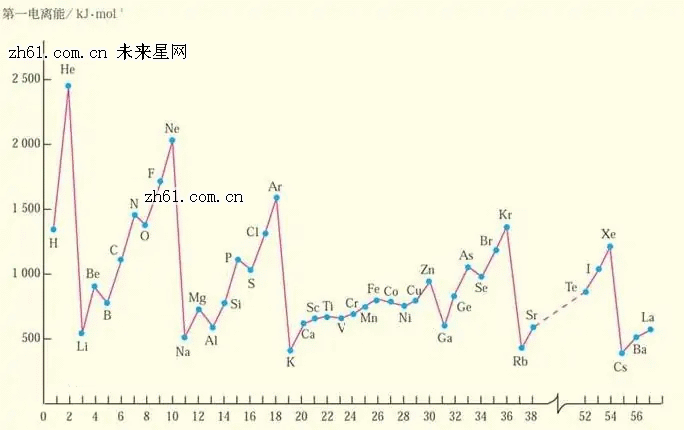
第一电离能周期性变化表
1.随着核电荷数的递增,元素的第一电离能呈现周期性变化。
2.总体上金属元素第一电离能较小,非金属元素第一电离能较大。
3.同周期元素第一电离能从左到右有增大的趋势。所以同一周期第一电离能最小的是碱金属元素,最大的是稀有气体元素。
4.同一周期内元素的第一电离能在总体增大的趋势中有些曲折。当外围电子在能量相等的轨道上形成全空(p0, d0, f0)、半满(p3, d5, f7)或全满(p6, d10, f14)结构时,原子的能量较低,元素的第一电离能较大。特例是第二主族的第一电离能大于第三主族,第五主族的第一电离能大于第六主族。
5.同一主族元素从上到下,原子半径增加,有效核电荷增加不多,则原子半径增大的影响起主要作用,第一电离能由大变小,元素的金属性逐渐增强。
6.同一副族第一电离能变化不规则

 更多
更多
 返回顶部
返回顶部 刷新页面
刷新页面 下到页底
下到页底